간세포암으로 오인된 단일 결절 호산구성 간농양
Solitary Eosinophilic Liver Abscess Mimicking Hepatocellular Carcinoma
Article information
Abstract
복부 초음파에서 저에코성 단일 결절이 확인되어 내원한 63세 남자 환자에서 CT, MRI와 같은 추가 영상검사를 통해 간세포암이 의심되어 간조직검사를 시행하였고, 호산구성 간농양을 진단한 증례이다. 호산구성 간농양은 다양한 영상학적 소견을 보일 수 있으며, 우리나라에서는 드물지 않은 질환으로 복부 초음파에서 단일 결절로 확인된 병변에 대해 추가적인 영상검사를 하기 전에 말초혈액 호산구 수치를 확인하는 것이 진단에 도움이 될 수 있겠다.
Trans Abstract
A 63-year-old male patient who presented with a hypoechoic solitary nodule on abdominal ultrasound was suspected of having hepatocellular carcinoma following additional imaging examinations of computed tomography and magnetic resonance imaging. To confirm the diagnosis of hepatocellular carcinoma, a liver tissue biopsy was conducted, and eosinophilic liver abscess was diagnosed. Eosinophilic liver abscess can present with various radiological findings and, in Korea, is not an uncommon condition. It may be beneficial to assess peripheral blood eosinophil counts before conducting additional imaging studies in cases where a solitary lesion is identified on abdominal ultrasound, as this can aid in the diagnosis.
서 론
국소 호산구성 간질환이란 간 실질에 호산구가 국소적으로 침윤하여 간조직 손상을 유발하는 질환으로서 조직병리 소견에 따라 문맥 주위와 간소엽에 호산구 침윤이 확인되나 정상적인 조직 구조를 유지하는 국소 호산구 침윤과 호산구 침윤으로 인한 염증과 간실질 파괴가 확인되는 호산구성 간농양으로 나눌 수 있다. 기생충 감염, 약물, 알레르기 질환, 특발성 호산구 증가증 등이 잘 알려져 있는 원인이며, 드물게 악성 종양이 있는 경우, 암의 전이 없이 간 실질에 호산구가 침윤하여 호산구 성 간농양을 형성하여 전이암과의 감별이 어려운 경우도 있다. 대부분 증상이 없거나 다른 질환에 대한 영상검사에서 우연히 발견되는 경우가 60% 정도로 보고되고 있다[1]. 특징적인 영상 검사 결과와 말초혈액 호산구 증가를 확인하면 호산구성 간농양을 의심해 볼 수 있으나 비전형적인 경우 영상검사만으로 진단이 어려운 경우가 있다. 복부 초음파에서 단일 결절로 나타나 종양성 병변과의 감별에 어려움이 있었던 증례를 기술하고자 한다.
증 례
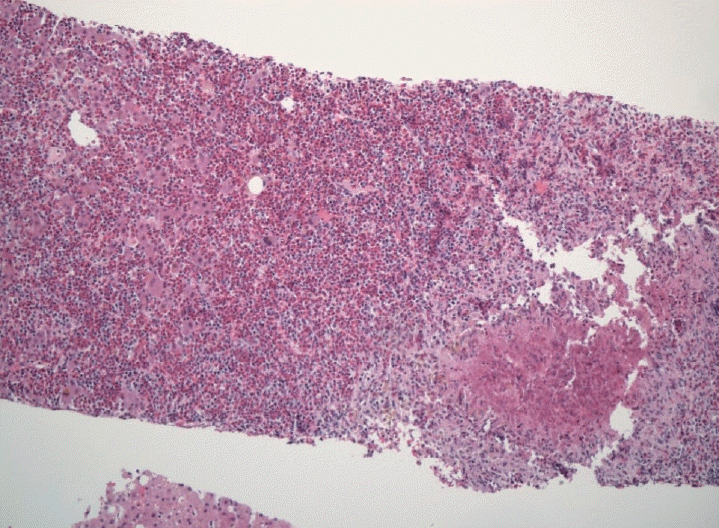
63세 남자 환자가 복부 초음파 검사에서 저에코성 결절이 발견되어 내원하였다. 환자는 3년 전 직장 신경내분비종양으로 내시경 점막절제술 후 주기적인 검사를 받고 있었으며, 1년 전 복부 초음파에서는 발견되지 않았던 결절이 새롭게 발견되었다. 3년 전 직장 신경내분비종양을 진단받으면서 시행했던 복부 초음파에서 지방간이 확인되었으며, 음주력과 흡연력은 없었다. 신체검진에서 키 171 cm, 몸무게 80 kg, 체질량지수 27 kg/m2로 비만이 확인되었으며, 그 외 다른 소견은 없었다. 복부 초음파에서 간실질 에코가 증가해 있고, 간신대조(hepatorenal contrast)가 보이는 지방간이 확인되었다. 우늑간스캔에서 간의 6분절에 1.9 cm의 경계가 명확한 저에코성 결절이 확인되었으며, 도플러 초음파에서 결절 내부에 혈류는 확인되지 않았다(Fig. 1). 새롭게 발견된 병변으로 신경내분비종양의 간 전이 가능성을 고려하여 역동적 조영증강 전산화단층촬영(computed tomography, CT) 검사를 진행하였다. CT 검사에서 동맥기에 약하게 조영증강이 되고 문맥기에는 테두리 조영증강이 확인되나 지연기에는 다시 결절 전체가 조영증강 되는 비특이적인 양상을 보여(Fig. 2) 추가적으로 간세포특이조영제 자기공명영상(magnetic resonance imaging, MRI) 검사를 시행하였다. 동맥기에서 조영증강이 미약하게 확인되었으며, 문맥기에 결절 내부는 약하게 씻김 현상이 확인되나 테두리 조영증강을 보였다. 간담도기의 명확한 씻김 현상이 확인되었고 확산강조영상에서 고신호강도가 보여 CT, MRI 소견이 모두 일치를 보이지는 않았으나 MRI 검사 결과로는 간세포암이 의심되었다(Fig. 3). 혈액검사 결과에서는 혈색소 15 g/dL, 백혈구 7,400/mm3, 혈소판 210,000/mm3, 아스파르테이트아미노전달효소(aspartate transaminase) 30 U/L, 알라닌아미노전달효소(alanine transaminase) 36 U/L, 총빌리루빈(total bilirubin) 0.5 mg/dL, 알부민(albumin) 4.8 g/dL, 감마글루타밀전달효소(gamma glutamyl transferase) 40 U/L로 확인되었다. 알파태아단백(alpha-fetoprotein)은 정상이었으나, 호산구 수치가 9.6% (710/mm3)로 상승되어 있었다. 환자는 만성 B형 간염 혹은 C형 간염은 없었으며 간경변증도 없었다. 비만과 비알코올 지방간질환을 가지고 있기는 하였으나 간세포암의 위험인자로 생각되는 기저 질환은 없어서 확진을 위해 해당 병변에 대해서 초음파 유도하 간조직검사를 진행하였다. 병리검사에서는 호산구가 심하게 침윤한 호산구성 농양으로 진단되었다(Fig. 4). 호 산구성 농양으로 확인된 이후 기생충 감염 여부 확인을 위해 ELISA 검사를 하였고, 개회충(Toxocara canis) 항원에 대한 항체가 확인되었다. 특별한 증상을 호소하지 않았으나 환자는 평소 육회를 자주 섭취하는 식습관이 있다고 하여 톡소카라증(Toxocariasis)을 배제할 수 없었다. 치료를 위해 알벤다졸 400 mg을 1주일간 복용하였다. 3개월 후 추적 복부초음파에서 해당 결절은 사라졌고, 혈액검사에서 호산구 수치는 정상으로 회복되었다.
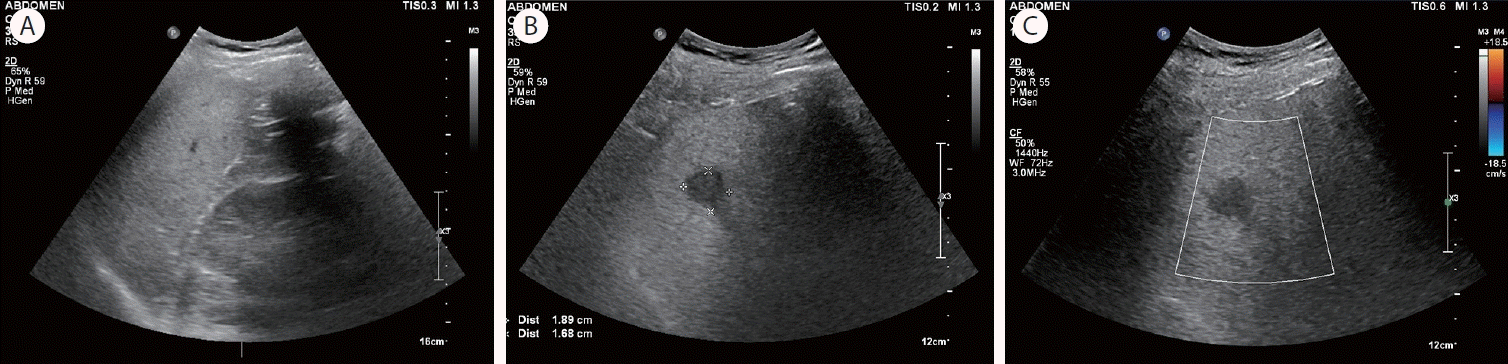
Abdominal ultrasound showed hepatorenal contrast (A). In the intercostal scan, a hypoechoic nodule measuring 1.9 cm in size was identified at S6 (B), and no blood flow was observed within the nodule on color Doppler (C).

Computed tomography showed a 1.9 cm-sized arterial enhancing nodule in S6. This nodule presented a non-specific finding of peripheral contrast enhancement during the portal phase and subsequent overall contrast enhancement during the delayed phase.
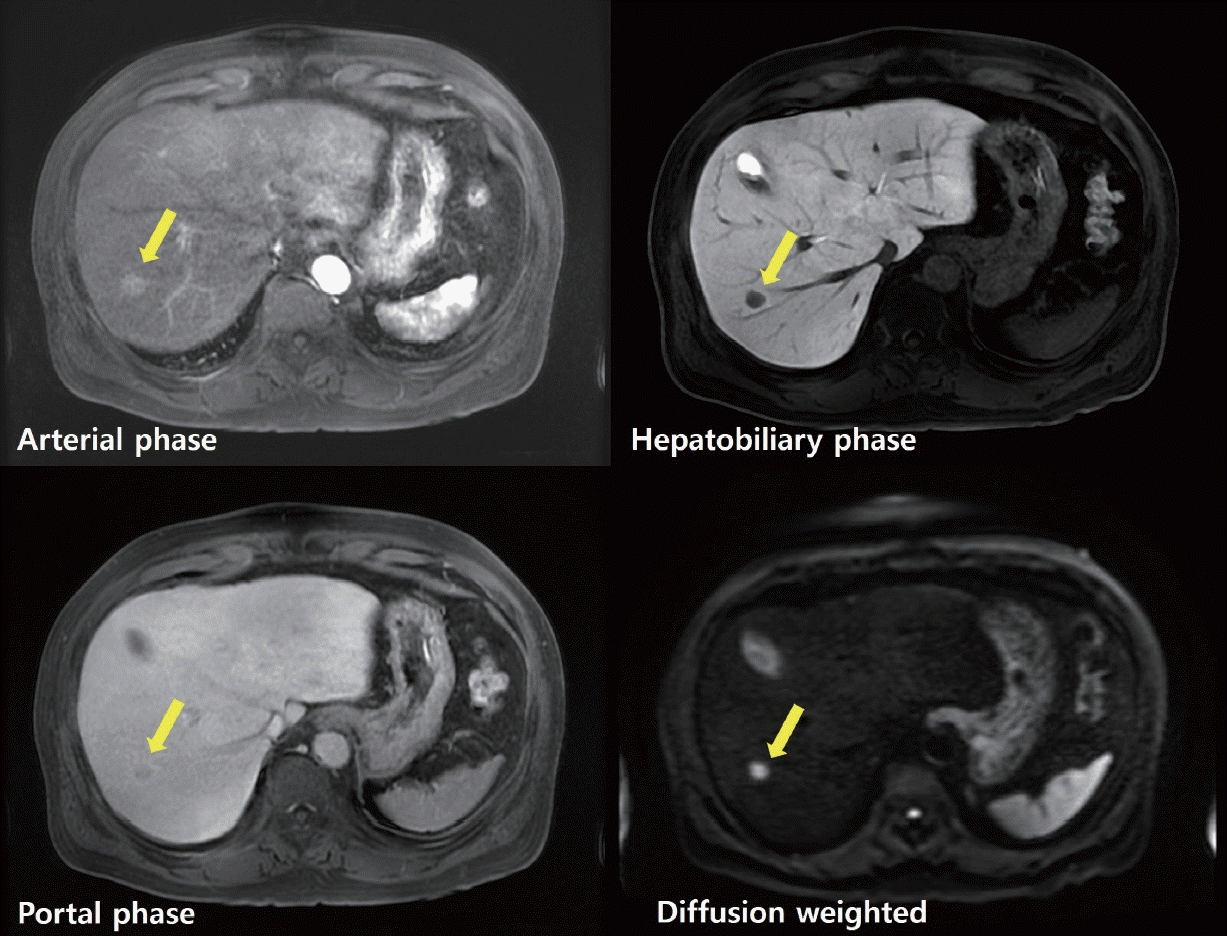
On magnetic resonance imaging, a lesion with arterial enhancement was identified. During the portal venous phase, its interior exhibited low signal intensity and peripheral enhancement. Significant washout was observed in the hepatobiliary phase, and high signal intensity was detected on diffusion-weighted images, raising suspicion of hepatocellular carcinoma.
고 찰
호산구성 간농양에서 나타나는 조직학적 특징인 호산구 침윤은 호산구 주성 인자가 그 원인으로, 기생충 감염이나 알레르기 반응으로 분비가 유발될 수 있다. 또한, 위암이나 담관암 등의 악성 종양에서 분비되는 호산구 주성 인자가 문맥을 통해 간으로 이동하여 호산구 침윤을 유발하는 경우 종양의 실제 전이 없이 간내 호산구 침윤만 나타나서 간 전이와 감별이 어려운 경우도 보고되고 있다[2]. 호산구 주성 인자 분비로 인해 일반적으로 호산구성 간농양을 가진 환자에서 말초혈액 호산구 증가증을 동반하는 경우가 많다고 알려져 있다[3].
호산구성 간농양은 대부분의 환자에서 무증상으로 우연히 복부 영상 검사에서 발견되는 경우가 많아서 초기에 임상적으로 호산구성 간농양을 의심하기는 어렵다. 병변을 발견할 당시 혈액검사에서 호산구 증가증이 확인되고, 복부 초음파에서 다발성의 크기가 작은 저에코성 병변으로 경계가 불분명한 원형 혹은 타원형의 결절로 나타난다면[4] 호산구성 간농양을 의심하고 호산구 증가증에 대한 원인 규명이 필요하다. 말초혈액 호산구 증가증의 원인으로 알레르기 질환이나 약물 알레르기가 높은 비율을 차지하고 있지만, 기생충 감염도 흔한 원인 중의 하나이다[5]. 하지만 복부 초음파에서 경계가 분명한 단일 병변으로 나타나며 영상 검사 당시 혈액검사 결과가 없다면 호산구성 간농양을 의심하기는 어렵다. 이러한 경우 악성 결절을 감별하기 위해 CT 혹은 MRI 검사를 시행하게 된다. 호산구성 간농양은 CT에서 대부분 2 cm 이하의 크기로 저음영을 보이며, 동맥기나 지연기보다는 정맥기에 가장 뚜렷하게 보인다. 하지만 드물게 동맥기에 조영증강이 되는 경우가 있는데 이런 경우 간세포암과의 구별이 어려워진다[1]. MRI 검사의 경우 T1 강조영상에서는 등신호 또는 약간 높은 고신호강도를 보이며, T2 강조영상에서는 약간 높은 고신호강도를 보인다. CT와 마찬가지로 경계가 불분명하며 지연기에서 저신호 강도를 보이기도 하지만, 염증이 심한 경우 테두리에 고신호강도를 보이기도 한다[6,7]. 하지만 간세포특이조영제 MRI에서 호산구성 간농양의 경우 문맥기, 지연기, 간담도기에 저신호 강도를 간세포암으로 오인될 수 있고, 우리나라는 국소 호산구성 간질환이 드물지 않게 발생하므로 환자의 혈중 호산구 수치를 확인하는 것이 진단에 도움이 될 수 있다[8].
호산구성 간농양은 영상검사만으로 진단이 어려우며, 경계가 분명한 단일 병변으로 복부 초음파에서 발견되는 경우 호산구성 간농양을 의심하기는 어렵다. 하지만 본 증례처럼 복부 초음파에서 경계가 분명한 단일 병변으로 나타나는 비전형적인 양상을 보이고 MRI에서 간세포암이 의심되는 병변에서 호산구성 간농양으로 진단되는 경우도 있어서 추가적인 영상검사를 진행하기 전에 혈액검사를 통해 말초혈액 호산구 수치를 확인하는 것이 진단에 도움이 될 수 있겠다.